Các dạng bài tập hóa học lớp 9 chương 1
Giải bài tập hóa học lớp 9 Chương 1: những loại hợp chất vô cơ
Video Giải bài tập Hóa 9 bài bác 1: tính chất hóa học tập của oxit. Khái quát về việc phân loại oxit – Cô Nguyễn Thị Thu (Giáo viên VietJack)
Bạn sẽ xem: giải bài bác tập hóa 9 chương 1
Với giải bài xích tập chất hóa học lớp 9 Chương 1: các loại hợp chất vô cơ Bạn đang xem: Các dạng bài tập hóa học lớp 9 chương 1
Tài liệu định hướng và những dạng bài tập chất hóa học lớp 9 Chương 1: những loại hợp hóa học vô cơ:
Các dạng bài xích tập chất hóa học 9 Chương 1: các loại hợp chất vô cơ lựa chọn lọc500 bài xích tập trắc nghiệm chất hóa học lớp 9 bao gồm lời giảiTổng hợp kiến thức Hóa học 9 Chương 1: những loại hợp hóa học vô cơ chi tiếtGiải bài xích tập hóa học 9 bài 1: đặc điểm hóa học tập của oxit. Khái quát về sự việc phân nhiều loại oxitBài 1 (trang 6 sgk hóa học 9): bao gồm oxit sau: CaO, Fe2O3, SO3. Oxit nào gồm thể chức năng được với:
a) Nước.
b) Axit clohiđric.
c) Natri hiđroxit.
Viết những phương trình bội phản ứng.
Lời giải:
a) số đông oxit chức năng với nước:
CaO + H2O → Ca(OH)2
SO3 + H2O → H2SO4
b) đều oxit tính năng với axit clohiđric:
CaO + 2HCl → CaCl2 + H2O
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
c) phần đông oxit tác dụng với dung dịch natri hiđroxit:
SO3 + NaOH → NaHSO4
SO3 + 2NaOH → Na2SO4 + H2O.
Bài 2 (trang 6 sgk chất hóa học 9): gồm có chất sau: H2O, KOH, K2O, CO2. Hãy cho thấy thêm những cặp chất nào bao gồm thể công dụng với nhau.
Lời giải:
Những cặp chất tác dụng với nhau từng song một:
H2O + CO2 → H2CO3
H2O + K2O → 2KOH
2KOH + CO2 → K2CO3 + H2O
KOH + CO2 → KHCO3
K2O + CO2 → K2CO3
Bài 3 (trang 6 sgk chất hóa học 9): Từ phần nhiều chất sau: can xi oxit, lưu huỳnh đioxit, cacbon đioxit, lưu hoàng trioxit, kẽm oxit, em hãy chọn 1 chất phù hợp điền vào những phản ứng:
a) Axit sunfuric + … → kẽm sunfat + nước
b) Natri hiđroxit + … → natri sunfat + nước
c) Nước + … → axit sunfurơ
d) Nước + … → canxi hiđroxit
e) canxi oxit + … → can xi cacbonat
Dùng những công thức hóa học để viết toàn bộ những phương trình phản bội ứng hóa học trên.
Lời giải:
a) H2SO4 + ZnO → ZnSO4 + H2O
b) 2NaOH + SO3 → Na2SO4 + H2O
c) H2O + SO2 → H2SO3
d) H2O + CaO → Ca(OH)2
e) CaO + CO2 → CaCO3
………………………………
………………………………
………………………………
Giải bài tập chất hóa học 9 bài 2: một số oxit quan liêu trọngA. Canxi oxitBài 1 (trang 9 sgk hóa học 9): Bằng phương pháp hóa học nào rất có thể nhận biết được từng chất trong mỗi dãy chất sau:
a) Hai hóa học rắn white color là CaO với Na2O.
b) Hai hóa học khí ko màu là CO2 và O2
Tham khảo: Thiền định là gì?
Viết mọi phương trình bội phản ứng hóa học.
Lời giải:
a) lấy một ít mỗi chất cho tác dụng với nước, tiếp nối đem lọc, nước lọc của các dung dịch này được thử bởi khí CO2 hoặc hỗn hợp Na2CO3. Nếu có kết tủa white thì chất lúc đầu là CaO, nếu không tồn tại kết tủa thì chất lúc đầu là Na2O. Phương trình phản nghịch ứng :
CaO + H2O → Ca(OH)2
Ca(OH)2 + CO2 → CaCO3 ↓ + H2O
Hoặc Ca(OH)2 + Na2CO3 → CaCO3 ↓ + 2NaOH
Na2O + H2O → 2NaOH
2NaOH + CO2 → Na2CO3 + H2O.
b) Sục hai chất khí không màu vào nhì ống nghiệm cất nước vôi Ca(OH)2 trong. Ống nghiệm làm sao bị vẩn đục, thì khí ban đầu là CO2, khí còn lại là O2.
PTPỨ: Ca(OH)2 + CO2 → CaCO3↓ + H2O
Bài 2 (trang 9 sgk chất hóa học 9): Hãy nhận ra từng cặp chất trong những nhóm hóa học sau bằng phương pháp hóa học:
a) CaO, CaCO3
b) CaO, MgO
Viết các phương trình bội phản ứng hóa học.
Xem thêm: Cập Nhật Các Loại Hạt Royal Canin Cho Mèo Trưởng Thành Phần, Cửa Hàng Bán 【 Royal Canin 】 Chính Hãng
Lời giải:
Nhận biết từng chất trong mỗi nhóm chất sau:
a) CaO cùng CaCO3.
Lẫy mẫu mã thử từng chất cho từng chủng loại thử vào nước khuấy đều.
Mẫu nào tính năng mạnh với H2O là CaO.
Mẫu còn lại không tan trong nước là CaCO3.
PTPỨ: CaO + H2O → Ca(OH)2
b) CaO cùng MgO.
Lấy chủng loại thử từng hóa học và cho tính năng với H2O khuấy đều.
Mẫu nào phản nghịch ứng bạo dạn với H2O là CaO.
Mẫu còn lại không công dụng với H2O là MgO.
PTPỨ: CaO + H2O → Ca(OH)2
Bài 3 (trang 9 sgk chất hóa học 9): 200ml dung dịch HCl có nồng độ 3,5mol/lit hòa tan đầy đủ 20g hỗn hợp CuO và Fe2O3.
a) Viết các phương trình phản ứng hóa học.
b) Tính trọng lượng của mỗi oxit bazơ tất cả trong các thành phần hỗn hợp ban đầu.
Lời giải:
VHCl = 200ml = 0,2 lít
nHCl = 3,5 x 0,2 = 0,7 mol.
Gọi x, y là số mol của CuO với Fe2O3.
a) Phương trình phản bội ứng chất hóa học :
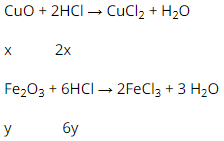
b) tự phương trình phản bội ứng bên trên ta có:
nHCl (1) = 2.nCuO = 2x mol
nHCl (2) = 6.nFe2O3 = 6y mol
⇒ nHCl = 2x + 6y = 0,7 mol (∗)
mCuO = (64 + 16).x = 80x g; mFe2O3 = (56.2 + 16.3).y = 160y g
Theo bài: mhỗn hòa hợp = mCuO + mFe2O3 = 80x + 160y = 20g
⇒ x + 2y = 0,25 ⇒ x = 0,25 – 2y (∗∗)
Thay x vào (∗) ta được: 2(0,25 – 2y) + 6y = 0,7
⇒ 0,5 – 4y + 6y = 0,7 ⇒ 2y = 0,2 ⇒ y = 0,1 mol
Thay y vào (∗∗) ta được: x = 0,25 – 2.0,1 = 0,05 mol
⇒ mCuO = 0,05 x 80 = 4g
mFe2O3 = 0,1 x 160 = 16g
(Lưu ý: lịch sự kì 2 các bạn mới học tập về Hệ phương trình phải bài này sẽ không giải theo cách đưa về hệ phương trình.)
………………………………
………………………………
………………………………
B. Lưu huỳnh đioxitBài 1 (trang 11 sgk chất hóa học 9): Viết phương trình hóa học cho mỗi đổi khác sau:
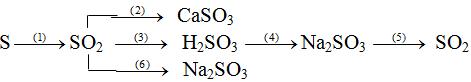
Lời giải:
(1) S + O2
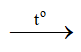
(2) SO2 + CaO → CaSO3
Hay SO2 + Ca(OH)2(dd) → CaSO3↓ + H2O
(3) SO2 + H2O ⇆ H2SO3
(4) H2SO3 + 2NaOH → Na2SO3 + 2H2O
Hoặc H2SO3 + Na2O → Na2SO3 + H2O
(5) Na2SO3 + H2SO4 → Na2SO4 + SO2 ↑ + H2O
Không đề nghị dùng bội nghịch ứng:
Na2SO3 + 2HCl → 2NaCl + SO2 ↑ + H2O do HCl dễ bay hơi phải khí SO2 thu được sẽ không tinh khiết.
(6) SO2 + 2NaOH → Na2SO3 + H2O
Hoặc SO2 + Na2O → Na2SO3
Bài 2 (trang 11 sgk chất hóa học 9): Hãy nhận thấy từng chất trong mỗi nhóm chất sau bằng phương pháp hóa học:
a) Hai hóa học rắn white color là CaO cùng P2O5.
b) Hai chất khí không màu là SO2 với O2.
Viết các phương trình hóa học.
Lời giải:
Nhận biết các chất sau:
a) CaO và P2O5
Lẫy mẫu mã từng hóa học và cho vào nước thu được 2 hỗn hợp Ca(OH)2 và H3PO4
Dùng quỳ tím mang lại vào những mẫu này.
Mẫu nào có tác dụng quỳ tím hóa xanh là Ca(OH)2 → hóa học rắn ban đầu là: CaO.
Mẫu nào làm quỳ tím hóa đỏ là H3PO4 ⇒ hóa học rắn thuở đầu là P2O5
PTHH: CaO + H2O → Ca(OH)2
P2O5 + 3H2O → 2H3PO4
b) SO2 với O2.
Lấy chủng loại thử từng khí.
Lấy quỳ tím ẩm cho vào từng mẫu mã thử. Mẫu nào làm quỳ tím hóa đỏ là SO2, còn lại là O2.
PTHH: SO2 + H2O → H2SO3
Bài 3 (trang 11 sgk hóa học 9): có những khí ẩm (khí tất cả lẫn hơi nước): cacbon đioxit, hiđro, oxi, lưu hoàng đioxit. Khí nào rất có thể làm khô bằng canxi oxit? Giải thích.
Lời giải:
Điều khiếu nại chất có thể làm khô được phần đông chất khác:
+ bắt buộc hút ẩm được.
+ Không tác dụng với chất được làm khô.
Ta thấy CaO có tính hút ẩm (hơi nước) tạo ra thành Ca(OH)2, đồng thời là một trong oxit bazơ (tác dụng cùng với oxit axit). Vì vậy CaO chỉ dùng làm khô các khí độ ẩm là hiđro ẩm, oxi ẩm.
………………………………
………………………………
………………………………











